Vydání 1/ 2026
VĚDA
-
Zobrazení: 0
LENKA BACHRATÁ: EPIGENETIKA. JAK PROSTŘEDÍ A ZKUŠENOSTI FORMUJÍ NAŠI OSOBNOST, CHOVÁNÍ, SOCIÁLNÍ ROLI I NEMOCI
SOUHRN:
Zdá se, že doba, ve které jsme věřili, že naši osobnost, chování a nemoci předurčují naše geny, pomalu ale jistě končí. Výzkum na poli epigenetiky prokazuje, že informace obsažená v genech je pod významným regulačním vlivem aktuálního prostředí a gen tedy neobsahuje zdaleka tak konkrétní informaci, jak jsme se dlouho domnívali.
I když prostředí nedovede ovlivnit strukturu genu, má přes chemické (epigenetické) modifikace zásadní vliv na to, jestli a jak se informace obsažená v genu vyjádří. Epigenetické modifikace nám umožňují učit se ze zkušeností a adaptovat naše těla, chování i metabolismus na aktuální prostředí a přežití.
Současně jsou však tyto modifikace spojovány i s rozvojem nemocí a zkráceným přežitím. Jak tomuto zásadnímu konfliktu rozumět?
Výzkum na poli sociální a behaviorální epigenomiky nabízí širší pohled na význam epigenetických modifikací nejen pro adaptaci a přežití jedince a sociální skupiny, ale i pro adaptaci jedince na jeho roli v sociální hierarchii a tím i na rovnováhu a přežití komplexních biologických systémů. Tento pohled může vnést do porozumění zdraví a nemoci dost odlišný význam.
SUMMARY: BACHRATA, L.: EPIGENETICS: HOW THE ENVIRONMENT AND LIFE EXPERIENCES INFLUENCE OUR PERSONALITY, BEHAVIOR, SOCIAL ROLE AND DISEASES- PSYCHOSOM 2024; 22 (2), PP. 102- 115
The era of strong belief in gene influence on our personality, behavior and diseases seems to be getting to the end. Scientific evidence in the field of epigenetics suggests significant environmental regulatory influence on gene expression. Epigenetic research shows that genes do not carry such rigid information as it had been originally proposed. Though environmental stimuli do not change gene structure, they can influence gene expression by maens of chemical epigenetic modifications.
Epigenetic modifications help us learn from our experience and adapt our bodies, behavior and metabolism for current environment and survival.
Surprisingly are these modifications concurrently associated with disease development and shorter life expectancy. How should be this apperent conflict understood?
Research in the fields of social and behavioral epigenomics brings more complex understanding of the role of epigenetic modifications for individual and social group adaptation and survival, for formation of individual personality and social status in complex hierarchies and perhaps even for balance and survival of complex biological systems. This view could bring quite different perspective to understanding of health and diseases.
EPIGENETIKA: PROMĚNY GENETIKY V KONTEXTU EPIGENETICKÝCH MODIFIKACÍ
Původní představa, že naše geny určují, kdo jsme, jak se chováme a k jakým nemocem máme dispozici, se zdá být definitivně pohřbenou minulostí. Ještě před 30 lety jsme věřili, že „gen“ je konkrétní sekvencí DNA, která kóduje přesně definovanou informaci. To dnes již neplatí. Výzkumy potvrzují, že geny, tedy specifické DNA sekvence, obsahují jakousi nejednoznačnou informaci, která začne dávat konkrétní význam až v kontextu komplexních souvislostí a interakcí organismu s jeho prostředím.
Zdali a jak se informace obsažená v „genu“ propíše pod vlivem prostředí do našeho vzhledu, chování či metabolismu, je řízeno komplexním regulačním systémem epigenetických modifikací, které nezasahují do struktury DNA, ale různými chemickými a fyzikálními mechanismy ovlivňují proces přepisu DNA kódu do finální bílkoviny. Právě těmito regulačními mechanismy se zabývá obor zvaný epigenetika.
Dnes již víme, že jen méně než 2% naší DNA tvoří „geny“, tedy kódující sekvence, obsahující informaci, která se přepisuje do podoby konkrétní bílkoviny se specifickou funkcí v organismu. Více než 98% DNA je tzv. nekódující a vědci ji dlouho považovali za něco jako evoluční odpad. Výzkumy však prokazují, že tato nekódující DNA odpadem rozhodně není. U velké části tohoto materiálu již bylo prokázáno, že má zcela zásadní regulační vliv na expresi informace obsažené v „genech“.
U různých živočišných druhů je poměr kódující vůči nekódující (regulační) DNA různý a výzkumy naznačují, že čím složitější organismus a komplexnější prostředí, tím vyšší je podíl regulační DNA k té kódující (Moore, 2015). Z těchto pozorování se můžeme domnívat, že vysoká adaptační plasticita a schopnost učení se ze zkušenosti má vysokou biologickou prioritu.
Epigenetické výzkumy mají převratný potenciál a zásadně rozšiřují povědomí na poli medicíny a biologie. Týkají se totiž naprosto všeho a v mnoha oborech obrací naše dosavadní poznání vzhůru nohama. Pro správné porozumění těmto informacím je ale potřebné symbolicky vrátit člověka tam, kam patří: do přírody a do komplexních biologických a vztahových souvislostí.
EPIGENETICKÉ MECHANISMY V KOSTCE
Pro zájemce o hlubší porozumění technické stránce epigenetického procesu si dovolím na úvod shrnout základy školní genetiky.
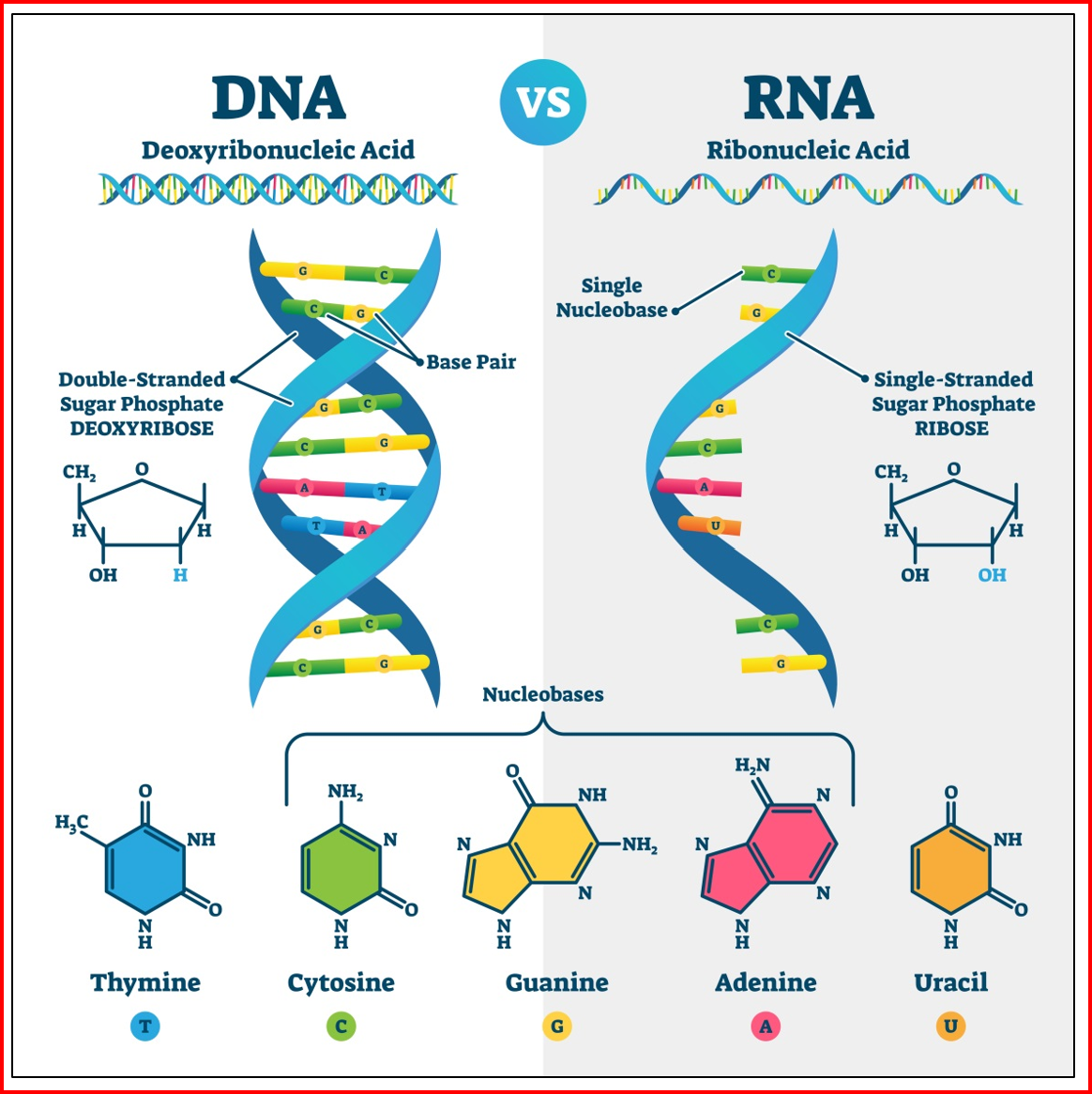 OBRÁZEK 1: ZÁKLADNÍ SCHEMATICKÁ STRUKTURA DNA A RNA. (ZDROJ: ADOBE STOCK, PLACENÁ VERZE)
OBRÁZEK 1: ZÁKLADNÍ SCHEMATICKÁ STRUKTURA DNA A RNA. (ZDROJ: ADOBE STOCK, PLACENÁ VERZE)
Naše genetická informace je uložená v buněčném jádru v podobě 23 párů chromozomů. Z každého páru pochází jeden chromozom od otce a druhý od matky. Základní strukturu chromozomu tvoří vlákno DNA, navinuté kolem bílkovin, zvaných histony. K těmto bílkovinám a terciární struktuře chromozomu se dostaneme později, protože kromě vytváření prostorové kompaktnosti mají i spoustu dalších důležitých funkcí. Pojďme ale nejdříve k principu genetické informace, který je uložen v DNA.
DNA všichni známe jako dvojitou šroubovici, složenou ze dvou vzájemně propojených vláken. Každé vlákno je tvořeno pomyslnou páteří, na které jsou přichyceny řady čtyř v různém pořadí opakujících se nukleotidů: adeninu, guaninu, tyminu a cytosinu. Toto pořadí vytváří pomyslný kód. Dvojice nukleotidů adenin-tymin a cytosin-guanin jsou tzv. komplementární, mají k sobě jakousi zvýšenou chemickou náklonnost. Snadno se spolu párují slabou vodíkovou vazbou, díky které drží dvojice vláken pohromadě jako zip. Aby se kód obsažený v pořadí nukleotidů mohl vyjádřit do formy konkrétní bílkoviny, musí se řetězce odzipovat a na stejném principu komplementarity překopírovat do kódu mediátorové RNA (mRNA). Jediným rozdílem je, že v RNA je tymin nahrazený uracilem.
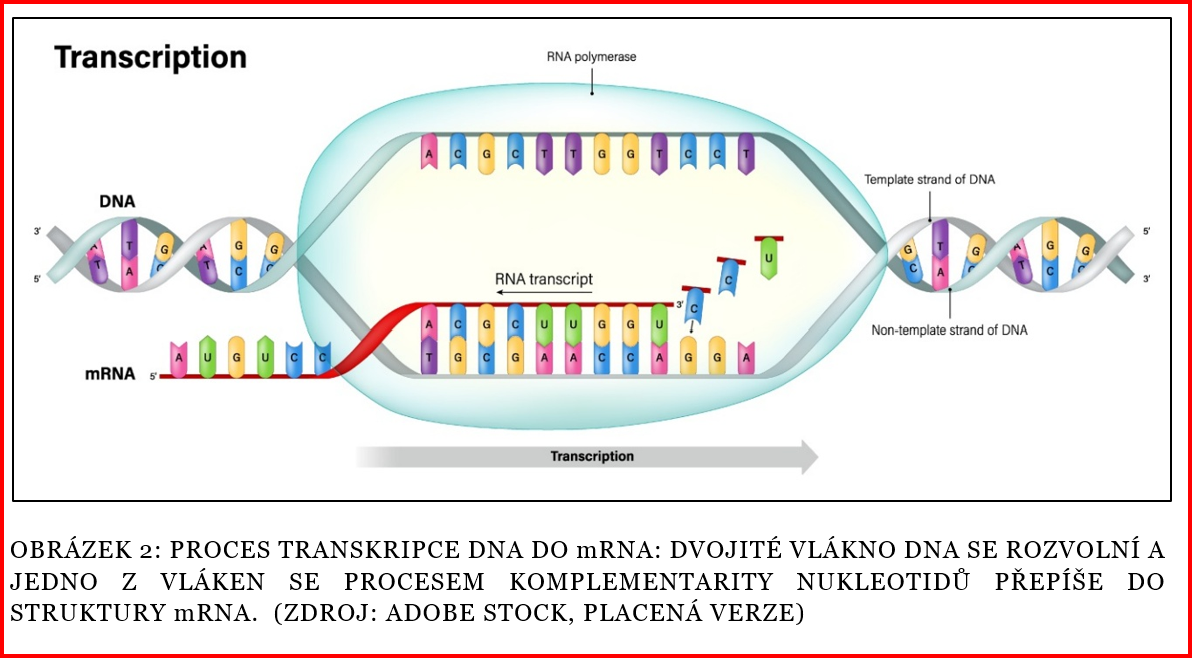
Tento proces kopírování informace z DNA do RNA se nazývá transkripce (přepis). Tato tzv. mRNA se dostává mimo buněčné jádro a v ribozomech je na základě tripletového kódu, kdy specifická trojice po sobě jdoucích nukleotidů kóduje specifickou aminokyselinu, překládána do podoby finální bílkoviny. Například triplet nukleotidů GCA (guanin, cytosin, adenin) kóduje aminokyselinu alanin, kód AGA zase arginin. Tento proces se nazývá translace (překlad). Z DNA kódu tedy procesem přepisu a překladu vzniká bílkovina složená z aminokyselin, kterých kód je určen sekvencí nukleotidů v konkrétním segmentu DNA.
Jak již bylo zmíněno výše, DNA vlákno vytváří kompaktní formu chromosomu díky své terciární struktuře, která je utvářena jeho navinutím kolem osmi bílkovin, zvaných histony. Základní strukturální jednotka osmi histonů s navinutou DNA se nazývá nukleosom. Pod mikroskopem působí nukleosom vizuálně jako klubíčko a celá DNA smotaná do nukleosomů vypadá jako řada korálků navlečená na šňůrce.
DNA vlákno drží na nukleosomech elektrostatickou silou, která vzniká mezi pozitivně nabitým histonem a negativně nabitou DNA.
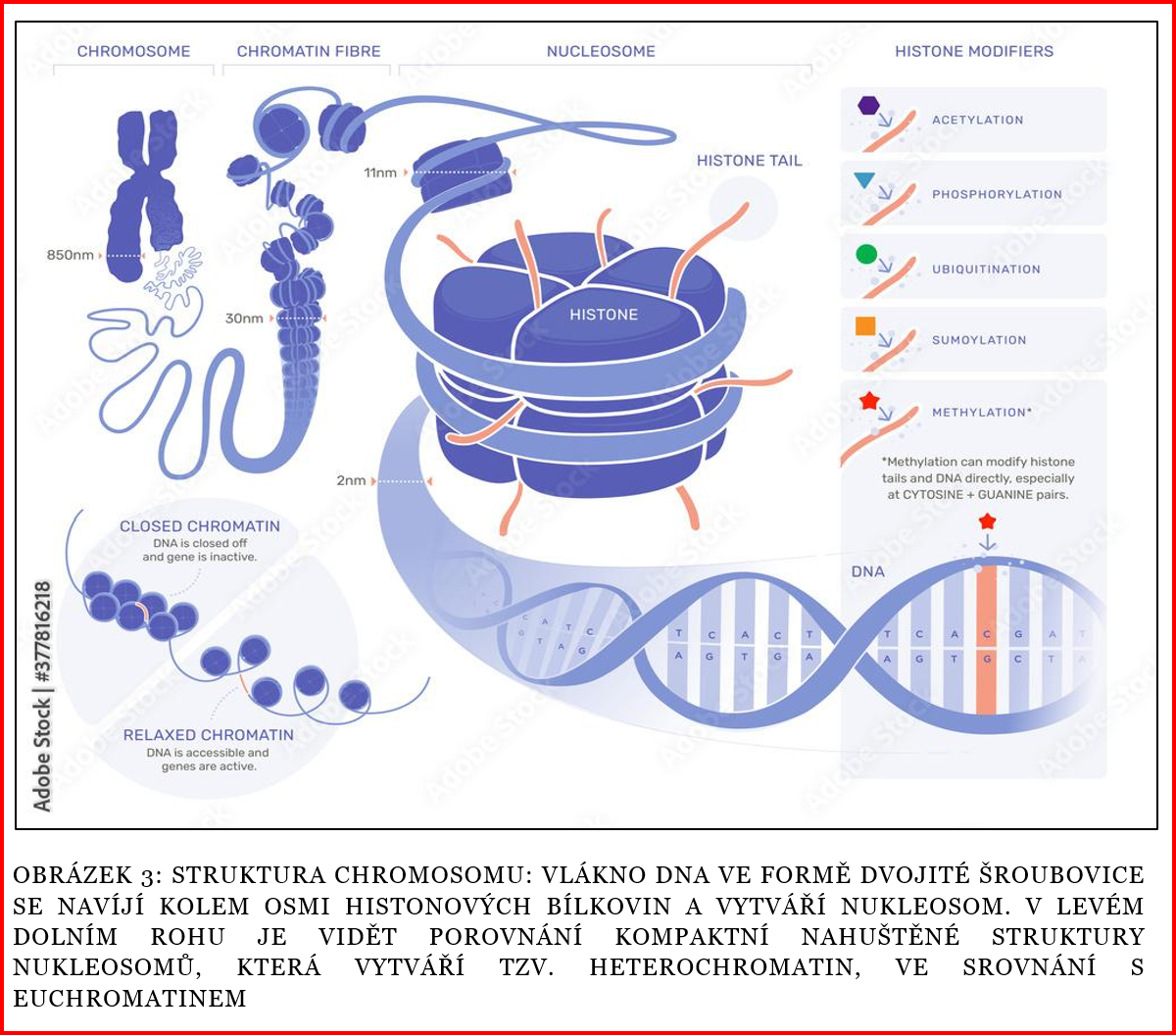
Jak lze vidět na obrázku vlevo dole, tyhle nukleosomové korálky mohou mít podobu těsné kompaktní formy, které říkáme heterochromatin, nebo podobu rozvolněné struktury, která se nazývá euchromatin. Tato dvojí podoba má význam nejen pro kompaktnost chromosomu, ale je zásadní i pro přístupnost DNA informace k přepisu, jak bude zmíněno níže.
Porozumění struktuře DNA i celého chromosomu je důležité pro pochopení toho, jak následné chemické modifikace mohou zasahovat do vyjádření informace, kterou jsme zdědili od svých rodičů.
JAK TEDY FUNGUJÍ EPIGENETICKÉ MECHANISMY?
Epigenetické mechanismy (EM) jsou souborem chemických značek a komplexních interakcí, zasahujících do procesu transkripce a translace na mnoha úrovních a mnoha způsoby. Soubor všech epigenetických modifikací jedné buňky se nazývá epigenetickým kódem a je vyjádřením jakési buněčné paměti, která se vytvořila interakcí buňky (případně souboru buněk v tkáni či celého organismu) se svým prostředím. Každá buňka či soubor buněk má svůj specifický epigenetický kód, který z části může být získán epigenetickou dědičností (viz níže), z části se vytvořil diferenciací buňky z pluripotentní ve specializovanou, a zčásti se dynamicky utváří neustálou interakcí s prostředím.
(Tato variabilita epigenetických kódů napříč tkáněmi je fascinující, protože potvrzuje schopnost učení se na úrovni buňky a nesmírnou plasticitu a dynamiku buněčných procesů. Nicméně značně komplikuje život vědcům, kterým znemožňuje zkoumat epigenetické procesy například v mozku jejich odvozováním od procesů v buňkách periferních (krevních či kožních). Tyto periferní buňky jsou sice pro potřeby výzkumu na žijících subjektech snadno dostupné k odběru, nicméně jejich epigenetický kód nelze použít pro pochopení toho, co se epigeneticky děje například v buňkách mozku.)
Pojďme se podívat detailně alespoň na některé z EM, které umožní základní náhled a současně mají srozumitelný význam pro porozumění tomuto složitému mechanismu (dále dle Mykura, 2023).
EM na úrovni DNA vlákna - metylace
Zřejmě nejznámější a současně technicky jednoduchou epigenetickou modifikací je tzv. metylace DNA, která negativně zasahuje do procesu transkripce.
Přepis kódu DNA do mRNA začíná ve specifickém místě, zvaném promotor. Když se metylová skupina (jeden atom uhlíku se třemi atomy vodíku) naváže na cytosin obsažený v tzv. CpG ostrůvku v tomto promotoru, dojde k zamezení přepisu a tím se celý další proces zastaví. Metylace DNA tedy zcela zabrání vyjádření informace obsažené v tomto „genu“. Efekt metylace DNA může být velice dlouhodobý a v některých případech může ovlivňovat fenotyp jedince po dobu celého života, nebo i života jeho potomků. Metylace DNA je totiž i jedním z mechanismů, díky kterým je možné zdědit zkušenosti svých předků, a to procesem tzv. transgenerační epigenetické dědičnosti (Fitz-James, Cavalli, 2022). Konkrétní praktický význam této modifikace bude zmíněn níže.
EM na úrovni histonu - acetylace
DNA vlákno drží v návinu na histonu díky elektrostatické síle. Dojde-li k acetylaci histonu, zruší se tím jeho pozitivní elektrický náboj a těsné navinutí DNA na histon se rozvolní (heterochromatin se změní na euchromatin, viz výše). Následkem toho dochází k mechanické dostupnosti části DNA k přepisu. Acetylace histonu je tak jedním z EM, které umožňují vyjádření DNA informace.
Na úrovni histonu probíhá celá řada EM, které souhrnně nazýváme histonovým kódem. Protože však záměrem tohoto článku není výčet všech známých EM, dovolím si nadšené zájemce o detaily odkázat na množství dostupné literatury.
EM na úrovni mRNA – mikroRNA, splicing
Kód mRNA získaný transkripcí podléhá mnoha dalším, tzv. posttranskripčním změnám, které mají významný vliv na translaci a vznik finální bílkoviny. Na této úrovni působí zejména tzv. malé nekódující RNA (sncRNA). Jednou z nich je mikroRNA, která dovede mRNA buď poškodit a tím úplně zamezit translaci, nebo je určena k tzv. fine-tuningu, čili jemnému vylaďování funkce (Issler a Chen, 2015). (V průběhu psaní tohoto článku byla objevitelům mikroRNA udělena Nobelova cena za medicínu a fyziologii, což potvrzuje ohromný význam poznání této struktury).
Z hlediska pochopení rozsahu naší plasticity je ale asi nejzajímavější EM tzv. „splicing“ (sestřih). Při něm dochází k „nasekání“ mRNA s cíleným vystřižením určitých segmentů (intronů) a následným spojením zbylých úseků (exonů). Výsledný řetězec mRNA se může významně lišit od původního a tím kódovat zcela odlišnou bílkovinu. Na první pohled se může zdát bizarní, proč DNA sekvence obsahuje úseky, které jsou určeny k vystřižení. Realita je ale fascinující, protože ve skutečnosti jde o pole vysoké plasticity. Proces tzv. alternativního splicingu totiž umožňuje, že z jedné RNA sekvence je možné různými variantami nasekání a opětovného spojení vytvořit buď podobné bílkoviny s mírně pozměněným účinkem, například varianty glukokortikoidního receptoru s různou citlivostí na kortizol (Anacker, Zunszain, Carvalho, Pariante – 2011), nebo i bílkoviny se zcela odlišnou funkcí, jako je například neurohormon a kalcium regulující transportér (Moore, 2015). Těch možností, jak jeden konkrétní řetězec mRNA nasekat a opět spojit (proces podobný editaci filmu), je totiž celá řada.
Pro lepší názornost si představme, že původní sekvence mRNA obsahuje informaci 1234. Alternativním splicingem je možné dosáhnout výsledné sekvence 123, 124, 234, 124, 12, 23, 34… tedy veškeré dostupné kombinace originálních segmentů. Dokonce se ukazuje, že ani nutně nemusí být následně spojeny v původním pořadí (Moore, 2015)! Takže variabilita výsledku je ve srovnání s úvodní dispozicí obrovská. Důležité je ovšem poznamenat, že variabilita není nekonečná a sekvenci 1234 nijak neproměníme na sekvenci 6789. V tomto pohledu je tedy „gen“ jakousi určenou dispozicí, tedy nabídkou surovin, ze které faktory prostředí podle potřeby mohou vybrat určitou kombinaci a „uvařit“ výsledný produkt.
Z jedné DNA sekvence tak mohou vzniknou vlivem rozdílných prostředí a odlišných potřeb organismu zcela rozdílné produkty.
K čemu to vlastně je?
Stejně jako informace obsažená v genu začíná dávat smysl až v konkrétním prostředí, tak začne dávat epigenetické poznání praktický smysl až v konkrétním kontextu.
Když se snažíme porozumět jeho významu v kontextu behaviorální biologie a evoluce, všechno nasvědčuje tomu, že epigenetické mechanizmy jsou prostředkem k naší adaptabilitě a plasticitě pod vlivem měnících se faktorů biologického a sociálního prostředí. Epigenetický kód je něco jako plastická buněčná paměť, vytvořená učením se ze zkušeností. Dalo by se říct, že nám pomáhá nestat se obětí své vrozené dispozice, ale dynamicky se adaptovat i na krátce trvající významné změny. Ultimátním záměrem by tedy mělo být přežití.
Má to ale samozřejmě množství různých háčků, ostatně jako vždy, když dospějeme k pocitu, že už něčemu rozumíme.
Jedním z nich je, že medicína stále více spojuje různé EM se vznikem nemocí, včetně nádorů. Vnímá je jako poruchy či chyby v programu a má tendenci hledat způsoby, jak nimi manipulovat „s léčebným úmyslem“. Tenhle očividný rozpor je opravdu matoucí. Jak je možné, že mechanismus, který by nás měl podle zdravého rozumu adaptovat na přežití, současně způsobuje nemoc? Na tuhle otázku zatím nemáme relevantní odpověď. (A je otázkou, jestli si tuhle otázku někdo z vědců vůbec klade.) Minimálně v psychosomatickém pohledu je však důležité se jí zabývat, neboť vede k hypotéze, že by se na nemoc mohlo v jejím kontextu nahlížet jako na behaviorální strategii či vnímat ji jako specifickou informaci.
Hypotéza propojení nemoci se strategií přežití není však tak nesmyslná a nelogická, jak by se mohlo na první pohled zdát. Je spíše v rozporu s přesvědčením západní medicíny, která nemoc prezentuje jako poruchu či poškození organismu, tedy jako problém, který je potřeba odstranit či opravit. Když však změníme optiku a začneme vnímat kontext, u mnoha „geneticky podmíněných“ nemoci najdeme původní adaptační záměr, který přivedl svého nositele k nemoci tím, že se změnil kontext prostředí. (více viz níže, v souvislosti s hemochromatózou).
Vraťme se ale k epigenetice a jejím adaptačním záměrům.
EPIGENETICKÉ UČENÍ: NAŠE BUŇKY SE DOVEDOU UČIT Z VLASTNÍ ZKUŠENOSTI
Jeden zajímavý výzkum na slimácích hezky demonstroval, jak opakované negativní zkušenosti ovlivňují naše dlouhodobé chování na epigenetické úrovni.
Výzkumníci pozorovali, že když slimák dostal ránu elektrickým proudem, zareagoval na následný neutrální dotek úlekovou reakcí. Tato nadměrná reaktivita následně odezněla v průběhu několika hodin.
Když ale slimák dostával sérii několika elektrických šoků denně po dobu dvou týdnů, úleková reaktivita na neutrální podnět přetrvávala po dobu několika měsíců. Výzkumníci prokázali, že toto behaviorální učení z opakované zkušenosti proběhlo na epigenetické úrovni (na rozdíl od krátkodobé reaktivity, která byla reflexní). Když totiž vědci podali slimákovi antibiotika inhibující proteosyntézu (tvorbu bílkovin), k tomuto učení z opakované negativní zkušenosti nedošlo.
Tento příklad velice hezky demonstruje, že jedna vlaštovka sice jaro nedělá, ale z opakované negativní zkušenosti se stává negativní rys prostředí, ze kterého je v rámci přežití důležité se poučit a zvýšit ostražitost. Opakované negativní zkušenosti tedy epigeneticky mění naše střednědobé chování ve smyslu adaptace na nepříznivé prostředí. Současně je však úlevné poznání, že po určitém období návratu „bezpečného“ prostředí tato nadměrná reaktivita opět odezní a slimák dovede s odstupem opět přijmout neutrální dotek bez nadměrné stresové reakce.
Mnohé výzkumy však prokazují, že negativní zkušenosti ve specifických obdobích života mohou ovlivnit chování (a taky celkový fenotyp, zdravotní dispozici, imunitní funkce, metabolismus...) i po mnohem delší dobu, tedy i po celý život jedince, dokonce mohou být přenášeny i na další generace potomků.
Těmto specifickým obdobím, ve kterých je enormní náchylnost k ovlivnění dlouhodobého chování, říkáme okna citlivosti. Mezi nejvíce vulnerabilní okna patří prenatální a perinatální období, kdy je jedinec zcela závislý na mateřské péči. Za další se považuje období puberty, ale je pravděpodobné, že oknem citlivosti je celé období dětství, kdy se nejvíce formuje naše osobnost a naše behaviorální strategie do dalšího života (Moore, 2015).
Na pre/perinatální okno citlivosti zaměřuje pozornost celá řada výzkumů. Mnoho z nich potvrzuje jeho formativní charakter. Například významný stres matky v těhotenství (vztahové problémy, zažívání násilí, ztráta blízké osoby, nutriční deficit, strach o dítě, obava z mateřství...) může zcela zásadně ovlivnit toleranci stresu dítěte v dalším životě, a to epigenetickým ovlivněním exprese glukokortikoidních receptorů (GR) v hypotalamu. Nedostatek těchto funkčních receptorů pak totiž znemožňuje, aby kortizol vyplavený v průběhu stresové reakce zpětnou vazbou snížil CRH (kortikotropin), který na centrální úrovni řídí aktivaci hormonální stresové reakce. V důsledku to tedy vede k tomu, že stresová reakce přetrvává výrazně déle, než by tomu bylo bez této časné negativní zkušenosti.
Podobný efekt, jaký má stres matky v těhotenství, mají i časné negativní zkušenosti po narození, zejména zanedbání, opuštění, násilné chování, chybění fyzického a emočního kontaktu s matkou, nedostatečně nutriční výživa a podobně. Kromě špatné tolerance stresu mají tyto adverzní zkušenosti vliv i na fyzický růst, stavbu těla, metabolismus, emoční stabilitu a dispozici k nemocem (Mousseau TA, Fox, 1998). Aktivita GR receptorů s následnou dysregulací HPP osy, způsobená časným traumatem, je již delší dobu přímo kauzálně spojována se vznikem deprese, poruchy kognitivních funkcí a poruch spánku (Anacker, Zunszain, Carvalho, Pariante – 2011).
A časně postnatálním obdobím to nekončí. Početné studie o tzv. ACEs (Adverse Childhood Experiences, neboli negativních zkušenostech z dětství) mluví jasnou řečí: časné a zejména opakované zkušenosti s fyzickým, emočním a sexuálním násilím, opuštění, fyzické a emoční zanedbání, špatná výživa, nepřijetí sociální skupinou a další objektivně i subjektivně negativně prožívané zkušenosti vedou k zásadnímu negativnímu vlivu na fyzické a duševní zdraví a ke zkrácenému přežití jedince.
A opět narážíme na zmíněný rozpor: to, co nás má adaptovat na přežití, má zřetelně negativní vliv na naše zdraví. Co si s tím počít?
V druhé polovině 20.století vyvinul klinický epidemiolog David Baker výzkumnou iniciativu pod názvem Vývojový původ zdraví a nemoci (Developmental Origins of Health and diseases). Dovolím si citovat jeho úvahu nad tím, co bylo zjištěno:
„Jsou dobré důvody, proč může být výhodou, aby tělo zůstalo plastické v průběhu vývoje. Umožňuje to produkci fenotypů, které lépe vyhovují pro přežití v jejich prostředí. Prenatální plasticita umožňuje jedincům získat přes matku něco jako „předpověď počasí“ a připravit je na prototyp světa, ve kterém budou muset žít. Špatně živená matka je předpovědí pro zlé časy a děti na to reagují menší tělesnou velikostí a změnou metabolismu, která jim umožní přežít v nedostatku. Tato plasticita tak dává lidskému druhu schopnost krátkodobé adaptace po dobu jedné generace.
Jestli je ale prostředí po narození jiné než to prenatální, dítě je pro něj „maladaptováno“, a dochází k vývojovému nesouladu.“
Negativní dětské zkušenosti přinášejí jedinci predispozici k ateroskleróze, obezitě či inzulínové rezistenci. Ty se ale nerozvinou u každého, pouze opět ve specifickém kontextu prostředí, například při sedavé práci a nutričním přebytku. Zdá se, že ony zkušenosti adaptují jedince a jeho metabolismus na těžký život v nedostatku, což je mu v prostředí dostatku spíše ke škodě, než k užitku (Moore, 2015).
Nechceme-li brát nesoulad mezi naší dispozicí a prostředím jako nepříznivý osud, je užitečné vnímat nemoc a různé nepříjemné tělesné pocity jako informaci a stimul ke změně chování, které nás dostane opět do rovnováhy.
Sociální biolog Robert M. Sapolsky však přichází s ještě komplexnějším evolučně-biologickým vysvětlením našeho epigenetického rozporu, které se nám z humánního a medicínského hlediska nemusí moc líbit. V knize Chování na mnoha důkazech jasně ukazuje, že evoluce a přežití nejsou o zdraví, dlouhověkosti a dobrých pocitech jednotlivce, ale o přenosu genetického materiálu a přežití druhu. Když prostředí jasně a intenzivně signalizuje krizi, nedostatek zdrojů a ohrožení, stává se omezení vzrůstu, metabolických nároků a délky života jedince adaptačním záměrem, kterého cílem je nasměrovat limitované zdroje do reprodukce a zachování druhu. Evoluce tedy v krizích a nedostatku selektivně upřednostňuje nikoli ty mužné, silné a krásně vzrostlé Adonise, ale naopak šlachovité a houževnaté zakrslíky s nízkou energetickou potřebou.
SOCIÁLNÍ EPIGENOMIKA – EPIGENETIKA SOCIÁLNÍCH SKUPIN
Sociální epigenomika je fascinujícím oknem do sociální biologie, která má zásadní přesah i pro porozumění lidské biologie a „zdraví“. S vědomím, že epigenetiku v dalších úvahách použiji spíš jako oslí můstek, pokusím se posunout pohled na lidskou fyziologii a zdraví ještě víc z optiky medicínské na optiku sociálně-biologickou.
Jak již bylo naznačeno výše, když se díváme na člověka v kontextu biologie, je jen stěží udržitelné medicínské přesvědčení, že hlavním záměrem homeostatických (alostatických) mechanismů lidského těla je „zdravotní“ rovnováha jednotlivce. Jakkoli může být pro nás těžké či neobvyklé to přijmout, jsme součástí komplexního biologického systému, pro který je prioritou rovnováha tohoto vyššího systému. A záměrem našich osobních regulačních mechanismů je neustále se dolaďovat k tomuto vyššímu systému, což vyžaduje schopnost dobré mimovědomé intuitivní vnímavosti a rovněž reaktivity našeho stresového (adaptačního) systému, nikoli trvalý nereaktivní stav meditativní rovnováhy, po jakém touží medicínské normy. Každý jedinec je v neustálém dynamickém adaptačním procesu, a proto nemáme šanci porozumět jeho fyziologii, dokud nerozumíme kontextu jeho prostředí a vztahů.
Sociální biologie přináší i důležitý pohled interindividuální variability, související se sociální rolí.
I když medicína tvrdí, že každý člověk je biologicky stejný, a tudíž má právo nastavit pro každého stejné fyziologické normy, výzkumy na poli sociální biologie a epigenomiky mají dost odlišný náhled.
V komplexních hierarchizovaných sociálních systémech je totiž funkční variabilita jejich členů smysluplným adaptačním záměrem a souvisí s jejich sociální rolí. V některých případech je dispozice k sociální roli zděděná, jinde se utváří v průběhu života vlivem prostředí, výživou či sociálními interakcemi epigeneticky (Guerrero, Fickel, Benheiem, Weyrich, Johns, 2020).
Ukázkovým příkladem epigenetického formování sociální role jsou včely. Může se to zdát překvapivé, ale larvy včelích dělnic i královny mají zcela totožnou DNA. Faktorem, který rozhoduje, ze které larvy se stane dělnice a ze které královna, je specifická výživa. Z larvy živené mateří kašičkou se vyvine včelí královna, z ostatních se stávají dělnice. A výsledný rozdíl je v mnoha ohledech zásadní: královna je daleko větší, plodná a žije až pětkrát déle ve srovnání s dělnicemi, které jsou menší a neplodné. Dělnice zas na rozdíl od královny mají na nohou pylové košíčky, které jsou pro jejich práci nezbytné (Moore, 2015). Královna i dělnice jsou pro fungování včelstva nezbytné, každá má svou specifickou roli pro funkci komplexního systému včelstva (Moore, 2021).
V sociálních systémech savců není fenotypová odlišnost tak zřetelná jako u včel a u různých živočišných druhů se podíl vrozené dispozice a dynamické epigenetické plasticity liší. Například sociální status jedince ve smyslu dominance či podřízenosti je často dán interakcemi jedince s prostředím a výsledek je podmíněný tělesnými danostmi (velikostí, silou), sociální podporou, výživou a dalšími faktory. Sociální status je ale významný i pro fyziologii a zdraví, protože jedinci s vyšší pozicí mají přednostní přístup ke zdrojům, což je zásadní pro jejich výkonnost, délku života a reprodukční úspěch. V stabilních sociálních hierarchiích, kde nejsou dominantní jedinci vyzýváni a ohroženi těmi podřízenými, bývají podřízení jedinci vystavováni agresivnímu chování ze strany dominantních, což má vliv na jejich zvýšenou hladinu glukokortikoidů, zhoršenou imunitu a horší přístup ke zdrojům potravy (Guerrero T.P., Fickel J., Benheiem S., Weyrich A, Johns, 2020).
Sociální biolog Robert M. Sapolsky ve své knize „Chování: Biologie člověka v dobrém i ve zlém“ krásně shrnul mnohé aspekty sociálního i přírodního prostředí, které mají vliv na naše chování a fenotyp, na strukturu a komplexnost sociální hierarchie i na sociální role v kontextu přežití.
Geografické charakteristiky, aspekty počasí, dostupnost zdrojů, velikost a uspořádání sociální skupiny, ohrožení predátory, kompetice skupin a mnoho dalších faktorů určuje, jaké strategie chování a sociální role projdou evoluční selekcí a jaké budou skrze EM prostředím upřednostňovány.
Podívejme se, jak faktory prostředí ovlivňují formování dominantních strategií přežití. Například v oblastech Asie, kde je hlavním zdrojem obživy pěstování rýže, je dominantní prosociální strategie a kolektivizmus, protože pro zabezpečení dostatku zdrojů je nevyhnutelná spolupráce větších skupin. Na obdělávání rýžových polí si musí vypomáhat i rodiny vzájemně, takže se evolucí prosadily strategie chování, které dovedou potlačit individuální potřeby a tolerovat jinakost. Jen v malých oblastech Asie, kde se pěstuje pšenice, se však překvapivě prosadily strategie individuální, kde je hlavním rysem schopnost spoléhat se hlavně na sebe. Podobně je tento druh strategie dominantní v horských oblastech a lokalitách, kde je hlavním způsobem obživy lov, případně kde je vysoká míra kompetice o zdroje.
Kolektivistická nebo individualistická strategie se neprojevuje pouze v chování. Specifické odlišnosti můžeme pozorovat i ve stavbě těla, svalovém napětí, v odlišném metabolismu, imunitní reaktivitě i rozdílné dispozici k nemocem, proto je téma dominantní strategie jedince důležitá i pro medicínu.
Je velice důležité uvědomit si, že všichni opravdu nejsme stejní. Mozaika vrozené dispozice a epigenetického kódu určeného naší zkušeností je zdrojem obrovské variability fenotypů. Každý máme svou vrozenou dispozici k určitému typu chování, tělesné stavbě a metabolismu, která je do určité míry plastická v kontextu aktuálního prostředí, ale ta míra není neomezená. Zdá se, že máme určitou míru vrozeného předurčení (dispozice), které je dobré rozumět a snažit se s ní být v souladu, nikoli proti ní bojovat a pokoušet se ji vtěsnat do uměle stanovených univerzálních norem (úvaha autorky).
Zajímavý pohled na tyto vrozené odlišné dispozice přináší i poznání související s variabilitou dopaminového receptoru, která má rovněž geografickou vazbu (Sapolsky, 2020). Nejběžnější varianta dopaminového receptoru D4 je 4R, která se vyskytuje u poloviny Východoasiatů a Američanů evropského původu. Varianta 7R je méně častá, produkuje receptor méně citlivý na dopamin a jeho nositele charakterizuje impulzivita, extroverze a vyhledávání nových podnětů. Vyskytuje se asi u 23 % Evropanů a Američanů evropského původu, v Asii však jen u 1 % populace. Vesnický pěstitel rýže by na dobrodruha tohoto typu asi koukal s nepochopením, ale díky těmto neposedným a zvídavým jedincům typu Kryštofa Kolomba se lidská civilizace rozvinula do současné mohutnosti a komplexity a zřejmě i zásluhou tohoto rysu přežila. Díky zvídavosti a dobrodružnosti hledáme nové a objevujeme neznámé, ale díky usedlosti, stálosti, trpělivosti a obětavosti máme co jíst a jsme schopni dovést své potomky k dospělosti. K přežití v komplexní společnosti potřebujeme, aby vedle sebe žili lidé s různými strategiemi, dispozicemi a sociálními rolemi.
Zkusme toto poznání aplikovat do medicíny a psychosomatiky. Dostaneme-li do vínku dispozici ke kolektivistickému chování a následně se přestěhujeme třeba do USA, budeme v této vysoce individualistické zemi tahat za kratší konec. Jestli se nám nepovede adaptovat se, zřejmě nás čeká despekt, izolace, bída, závist, vyšší nemocnost a kratší život.
Jestliže získáme vrozenou dispozici dobrodruha, můžeme při troše štěstí založit vysoce úspěšný byznys, ale také se ve dvaceti zabít na motorce. Když ale s touhle neposednou povahou uvízneme v kanceláři na 10 hodin denně, je velká šance, že nedostatek dopaminové aktivity začneme zajídat či zapíjet alkoholem a ve středním věku skončíme s obezitou, cukrovkou, infarktem, depresí a životní frustrací.
EXISTUJÍ OPRAVDU GENY PRO NEMOC, NEBO JE ZA KAŽDOU GENETICKOU DISPOZICÍ NĚJAKÝ PRIMÁRNĚ ADAPTIVNÍ ZÁMĚR?
Když se na genetiku a epigenetiku díváme očima biologie, je těžké uvěřit, že by evolucí prošla genetická informace, která by měla primární záměr jedince znefunkčnit či dokonce zabít. Jak již bylo zmíněno výše, někdy za epigenetickými adaptacemi vedoucími ke zkrácenému přežití či jinému fyzickému omezení můžeme najít smysl související s přežitím druhu či komplexního biologického systému. U jiných „geneticky podmíněných nemocí“ lze zas vystopovat, že dotyčný gen měl (či stále má) v určité historické, geografické či jiné souvislosti evoluční výhodu ve smyslu přežití.
Podívejme se například na hemochromatózu, geneticky podmíněnou nemoc, při které se hromadí železo v organismu. Jestli hladina železa v organismu překročí určitou míru, začne se železo usazovat v orgánech (játrech, slinivce, mozku, svalech...) a poškozovat je. V subkritickém množství je však vysoká hladina železa výhodou, protože zvyšuje hladinu hemoglobinu a tím i schopnost organismu dodávat tkáním víc kyslíku a umožnit nositeli genu vyšší fyzický výkon. Proto lze geny pro hemochromatózu najít ve vysoké četnosti u vrcholových sportovců, pro které jsou velkou kompetitivní výhodou (Kardasis, 2023 a Drishti, 2023). Většina genů pro hemochromatózu pochází z Irska a Skandinávie, takže když popustíme uzdu fantazii, je možné, že jejich nositelé jsou potomkové Vikingů či jiných válečníků, kterým tento gen přinášel výhodu větší síly a vytrvalosti v bojích a při zraněních spojených s krvácením jim zvyšoval šanci přežít. Posaďte však válečníka do kanceláře za počítač a uvidíte, co s tělem dovede nadělat konflikt mezi vrozenou dispozicí a neodpovídajícím prostředím.
ÚVAHY NA ZÁVĚR: CO SI Z TOHO VŠEHO VZÍT PRO PSYCHOSOMATIKU A MEDICÍNU?
Když vytrhneme pozorovaný objekt či úkaz z kontextu širších souvislostí, dobereme se ke zcela jiným pozorováním a závěrům, než když pozorujeme v kontextu.
Abychom mohli rozumět člověku, jeho chování i jeho zdraví, potřebujeme ho vrátit zpět do přírody a do komplexních biologických a sociálních souvislostí.
Epigenetické poznání má velký potenciál v tom, že konečně dovedeme rozumět tomu, jak moc jsme plastičtí a adaptabilní a jak nesmírná je naše schopnost učení se ze zkušeností. Současně však naznačuje i naše limity související s vrozenou dispozicí. Ta však nutně nemusí být omezením, když se pokusíme ji vnímat a přijmout jako svou podstatu, výhodu a cestu k hledání svého potenciálu a záměru v kontextu fungování sociální skupiny a komplexního biologického systému.
Naši osobnost, tělo, chování, metabolismus a sklon k nemocem formují naše genetické dispozice, naše životní zkušenosti i zkušenosti našich předků, prostředí, vztahy, naše sociální role a konflikty naší dispozice s přírodním a sociálním prostředím, s pravidly a potřebami společnosti. Porozumění těmto souvislostem nám může pomoci nahlížet na nemoc a tělesný příznak dost odlišnou optikou.
Když pozvedneme zrak od mikroskopu a přesuneme pozornost od detailu ke komplexním biologickým souvislostem, možná se nám povede vnímat nemoc jako jakýsi regulační mechanismus či důležitou informaci.
Je čas přijmout, že jsme neoddělitelnou součástí sociálních a biologických systému, kterých rovnováha a přežití jsou prioritou před našim „zdravím“. A že „zdraví“ je vlastně jakýsi umělý konstrukt, který odráží schopnost neustálého dynamického procesu intuitivní vnímavosti a kontinuálních adaptací na potřeby komplexních sociálních a biologických systémů.
POUŽITÁ LITERATURA:
1. Anacker C, Zunszain PA, Carvalho LA, Pariante CM. The glucocorticoid receptor: pivot of depression and of antidepressant treatment? Psychoneuroendocrinology. 2011 Apr;36(3):415-25. doi: 10.1016/j.psyneuen.2010.03.007. PMID: 20399565; PMCID: PMC3513407.
2. Drishti Thakkar 1 , Marc Sicova, Nanci S Guest, Bibiana Garcia-Bailo, Ahmed El-Sohemy: HFE Genotype and Endurance Performance in Competitive Male Athletes. Med Sci Sports Exerc. 2021 Jul 1;53(7):1385-1390. doi: 10.1249/MSS.0000000000002595.
3. Fitz-James, M.H., Cavalli, G. Molecular mechanisms of transgenerational epigenetic inheritance. Nat Rev Genet 23, 325–341 (2022). https://doi.org/10.1038/s41576-021-00438-5
4. Guerrero T.P., Fickel J., Benheiem S., Weyrich A, Johns P, Epigenomics and gene regulation in mammalian social systems. Current Zoology, 2020 Jun, 66(3), 307-319.
5. Issler O, Chen A. Determining the role of microRNAs in psychiatric disorders. Nat Rev Neurosci. 2015 Apr;16(4):201-12. doi: 10.1038/nrn3879. PMID: 25790865.
6. Kardasis William, Ethan R. Naquin , Richa Garg, Tejas Arun, Jyotsna S. Gopianand, Eshani Karmakar: The IRONy in Athletic Performance. Nutrients 2023, 15, 4945, Published: 28 November 2023
7. Moore, David S.: The Developing Genome: An Introduction to Behavioral Epigenetics. Oxford University Press, 2015, New York, USA
8. Mousseau TA, Fox CW. The adaptive significance of maternal effects. Trends Ecol Evol. 1998 Oct 1;13(10):403-7. doi: 10.1016/s0169-5347(98)01472-4. PMID: 21238360.
9. Mykura, Charlote: Epigenetics: How Environment Changes Your Biology. The Great Courses, 2023, USA.
10. Rodrigo G. Arzate-Mejía, Isabelle M. Mansuy: Epigenetic Inheritance: Impact for Biology and Society—recent progress, current questions and future challenges. Environmental Epigenetics, 2022, 8 (1), 1-7
11. Sapolsky Robert M.: Chování: Biologie člověka v dobrém i ve zlém. Dokořán, 2020, Praha.
Do redakce přišlo 25.1.2025
K tisku zařazeno po recenzi 30.4. 2025
Konflikt zájmů není znám
INFORMACE O AUTORCE:
MUDr. Lenka Bachratá je praktická lékařka pro dospělé a psychoterapeutka, působící v psychosomaticky zaměřeném zdravotním centru Mind&Body v Bratislavě. V současnosti je v přípravě na psychosomatickou atestaci, ale psychosomatický a komplexní mezioborový pohled na zdraví a nemoci je její vášní již dlouhá léta.




