Vydání 1/ 2026
VÝZKUM
-
Zobrazení: 0
FIGUEROA J., RAJPOOT S. S., NEDBALOVÁ L.: PSILOCYBINEM ASISTOVANÁ PSYCHOTERAPIE JAKO POTENCIÁLNÍ INTEGRATIVNÍ PŘÍSTUP V LÉČBĚ IDIOPATICKÝCH STŘEVNÍCH ZÁNĚTŮ
Úzkostné a depresivní příznaky jsou u idiopatických střevních zánětů (IBD) velmi časté a významně zhoršují kvalitu života, adherenci k léčbě i průběh onemocnění.
Psychoterapie a antidepresiva prokazatelně zmírňují psychické symptomy, jejich robustní a konzistentní vliv na somatické ukazatele aktivity IBD je však zatím omezený. Nové poznatky o ose střevo–mozek, serotonergní signalizaci a autonomní regulaci naznačují, že psilocybin (agonista 5-HT₂A receptorů) by při podání ve strukturovaném psychoterapeutickém rámci mohl představovat duálně působící modalitu, která ovlivňuje jak psychické procesy, tak psychoneuroimunitní regulaci. Preklinická a raná klinická data podporují hypotézu protizánětlivých, neuroplastických a autonomně modulačních účinků, nicméně klinické důkazy účinku psilocybinem asistované psychoterapie (PAP) na aktivitu IBD v současnosti chybí. Cílem článku je shrnout poznatky o psychických komorbiditách u IBD, diskutovat limity současných přístupů a představit opatrný racionální rámec pro PAP jako potenciálně integrativní přístup působící na tělo i mysl, včetně klíčových bezpečnostních a proveditelnostních otázek pro budoucí studie.
KLÍČOVÁ SLOVA: idiopatické střevní záněty; osa střevo–mozek; úzkost a deprese; psilocybin; psilocybinem asistovaná psychoterapie.
SUMMARY: FIGUEROA J., RAJPOOT S.S., NEDBALOVÁ L.: PSILOCYBIN-ASSISTED PSYCHOTHERAPY AS A POTENTIAL INTEGRATIVE APPROACH IN THE TREATMENT OF INFLAMMATORY BOWEL DISEASE. PSYCHOSOM 2026; 23(1), PP.20-31
Anxiety and depressive symptoms are highly prevalent in inflammatory bowel disease (IBD) and are associated with reduced quality of life, poorer treatment adherence, and a less favourable disease course. While psychotherapy and antidepressants can improve psychological outcomes, evidence for a robust and consistent impact on somatic markers of IBD activity remains limited. Advances in gut–brain axis research, serotonergic signalling, and autonomic regulation raise the hypothesis that psilocybin (a 5-HT₂A receptor agonist), delivered within a structured psychotherapeutic model, could represent a dual-target intervention affecting both psychological processes and psychoneuroimmune regulation. Preclinical and early human data suggest anti-inflammatory, neuroplastic, and autonomic modulatory effects; however, clinical evidence for psilocybin-assisted psychotherapy (PAP) on IBD inflammatory activity is currently lacking. This article summarises current knowledge on psychological comorbidities in IBD, discusses limitations of existing approaches, and proposes a cautious mechanistic and clinical rationale for PAP as a potential integrative strategy, including key safety and feasibility considerations for future trials.
KEY WORDS: inflammatory bowel disease; gut–brain axis; anxiety and depression; psilocybin; psilocybin-assisted psychotherapy.
Obr. 1.:OSA STŘEVO- MOZEK u IBD
Obr. 1.:OSA STŘEVO- MOZEK u IBD

2. MECHANISMUS PAP U IBD
ÚVOD: IBD JAKO ONEMOCNĚNÍ TĚLA I MYSLI
Idiopatické střevní záněty (IBD), mezi něž patří Crohnova nemoc, ulcerózní kolitida a neklasifikované IBD, jsou autoimunitní chronická relabující onemocnění s významnými systémovými a psychosociálními dopady. Symptomy deprese postihují přibližně 25,2 % a symptomy úzkosti 32,1 % pacientů s IBD; zátěž je vyšší než v obecné populaci i oproti mnoha jiným chronickým onemocněním (Barberio et al., 2021). Psychické symptomy se pojí s horší kvalitou života, horší adherencí k léčbě a častějšími relapsy (Irving et al., 2021).
Biologická a inovativní léčba představuje zásadní pokrok v terapii IBD a významně snižuje zánětlivou aktivitu onemocnění i riziko relapsů. Přesto se ukazuje, že psychické obtíže, zejména úzkostné a depresivní symptomy, často přetrvávají i u pacientů v klinické remisi (Irving et al., 2021). Tyto potíže negativně ovlivňují kvalitu života, adherenci k léčbě i subjektivní prožívání nemoci a bývají nezávislým prediktorem horší prognózy.
Naopak psychoterapie a antidepresiva prokazatelně zlepšují kvalitu života a zmírňují depresivní a úzkostné symptomy, jejich vliv na samotnou aktivitu zánětu však zůstává nejednoznačný a spíše limitovaný (Paulides et al., 2021; Wang et al., 2023; Weston et al., 2024; Tiles-Sar et al., 2025). Souhrnná analýza psychologických intervencí u IBD (Cochrane 2025) potvrzuje malé, avšak klinicky významné efekty na kvalitu života, depresi a úzkost u dospělých bez konzistentního dopadu na ukazatele zánětu (Tiles-Sar et al., 2025). Tento nález zdůrazňuje potřebu komplexnějších, integrativních přístupů, které mohou současně ovlivnit psychické i somaticko-imunitní mechanismy.
V klinické praxi je důležitý systematický screening úzkostně-depresivní symptomatiky a její dynamiky v čase; hodnocení může být podpořeno i moderními metodami měření (Wohlberg et al., 2020).
V českém prostředí byla problematika psychických obtíží u IBD zpracována v přehledovém článku Minárikové a kol. a oslovena úvodníkem Bortlíka (Mináriková et al., 2025; Bortlík, 2025). Na tyto texty navazujeme a rozšiřujeme jejich rámec o terapeutickou perspektivu vycházející z poznatků psilocybinem asistované psychoterapie (PAP). Pojem „duální terapeutická perspektiva“ používáme k vyjádření dvojího cíle – ovlivnění psychických symptomů úzkosti a deprese a současně ovlivnění vybraných psychoneuroimunitních mechanismů souvisejících se zánětlivým onemocněním.

OSA STŘEVO–MOZEK: MECHANISTICKÉ MOSTY
Imunitně–neurální rozhraní
Periferní prozánětlivé cytokiny, jako TNF‑α, mohou být detekovány aferentními vlákny n. vagus, která přenášejí informace o střevním zánětu do jádra tractus solitarii. Zde jsou signály integrovány a dále předávány do vyšších center, včetně hypotalamu a limbického systému, kde mohou aktivovat HPA osu a měnit stresové odpovědi; současně dochází k ovlivnění neuroimunitních procesů v CNS (Bonaz et al., 2018; Sinagra et al., 2020).
Stresové osy
Chronická aktivace HPA osy a sympatiku zpětně ovlivňuje střevní imunitu a bariérovou funkci. Hormony a mediátory stresu, jako kortizol, adrenalin a noradrenalin, zvyšují permeabilitu střevní sliznice, mění aktivitu imunitních buněk a mohou tak přispívat k relapsům zánětu (Abautret-Daly et al., 2018; Sinagra et al., 2020).
Autonomní regulace
Parasympatikus prostřednictvím tzv. cholinergního protizánětlivého reflexu inhibuje produkci prozánětlivých cytokinů; porucha vagové aktivity byla v preklinických modelech spojena se zvýšenou náchylností ke kolitidě (Ghia et al., 2008; Abautret-Daly et al., 2018).
Mikrobiota a její metabolity
U pacientů s IBD je opakovaně popisována dysbióza s nižší abundancí bakterií produkujících SCFA (např. Faecalibacterium prausnitzii, Roseburia intestinalis) a nižší produkcí SCFA (zejm. butyrátu). Současně dochází ke změnám metabolismu tryptofanu – posun ke kynureninové dráze (aktivované např. prostřednictvím IDO při zánětu) snižuje dostupnost 5‑HT a mění 5‑HT signalizaci v GIT i CNS [21]. Novější i starší přehledové práce naznačují, že obnova mikrobiální rovnováhy (zvýšení SCFA, modulace tryptofanového metabolismu) může tlumit aktivitu HPA osy a příznivě ovlivňovat symptomy úzkosti a deprese u IBD (Sinagra et al., 2020; Carabotti et al., 2015; Gao et al., 2020; Abautret-Daly et al., 2018).
Integrovaný pohled
Propojení imunitních, neuroendokrinních, autonomních a mikrobiálních os vytváří obousměrný systém, v němž se psychický stres a střevní zánět mohou vzájemně potencovat. Tento mechanistický rámec současně poskytuje biologické ukotvení pro přístupy s duálním terapeutickým cílem současnou modulací psychického stavu a zánětlivých procesů (Mayer, 2011; Ge et al., 2022).
SOUČASNÉ TERAPEUTICKÉ MOŽNOSTI A JEJICH LIMITY
Současná léčba IBD směřuje v rámci treat‑to‑target (T2T) k dosažení klinické, endoskopické a histologické remise. Biologická a inovativní léčba výrazně snižuje aktivitu zánětu i riziko relapsů, péče o psychické obtíže však často probíhá odděleně – typicky formou psychoterapie (KBT, ACT, mindfulness) nebo adjuvantní psychofarmakoterapie, zejména SSRI/SNRI (Paulides et al., 2021; Bernabeu et al., 2021; Ferreira et al., 2024; Wang et al., 2023; Weston et al., 2024). Systematické přehledy a metaanalýzy potvrzují, že tyto přístupy zlepšují kvalitu života a snižují úzkostně‑depresivní symptomy, avšak jejich přímý vliv na somatickou aktivitu IBD je heterogenní a spíše limitovaný (Paulides et al., 2021; Wang et al., 2023; Weston et al., 2024; Tiles-Sar et al., 2025). V praxi tak vzniká „pečovatelská mezera“ a multimodální, koordinovaná péče je spíše výjimkou, přestože by z ní významná část pacientů profitovala.
Zmíněné podtrhuje potřebu modalit, které překlenou propast mezi psychickou a somatickou složkou – tedy přístupů skutečně duálních až holistických, působících jak na úrovni psychoneurální regulace, tak na úrovni imunologických a inflamatorních mechanismů.
SEROTONERGNÍ SIGNALIZACE A TRYPTOFANOVÝ METABOLISMUS
Tryptofanový metabolismus představuje důležitý most mezi střevní mikrobiotou, imunitním systémem a CNS. U zánětlivých stavů včetně IBD je popisován posun tryptofanového metabolismu směrem ke kynureninové dráze, což může ovlivňovat dostupnost serotoninu a neuroaktivní metabolity a souviset s afektivní dysregulací a poruchou stresové regulace Serotonin z enterochromafinních buněk přispívá k regulaci motility a sekrece GIT a podílí se na modulaci imunitních odpovědí; v CNS ovlivňuje afekt, kognitivní flexibilitu a interocepci (Gao et al., 2020; Abautret-Daly et al., 2018).
PSILOCYBIN – LÁTKA NA POMEZÍ BIOLOGIE A SPIRITUALITY
Historie a původ
Psilocybin je přírodní tryptaminový alkaloid v houbách rodu Psilocybe, tradičně využívaný v některých rituálních kontextech ve Střední a Jižní Americe. V moderní době byl izolován Albertem Hofmannem (1958) a v 50.–60. letech intenzivně zkoumán v psychiatrii; výzkum byl přerušen legislativní restrikcí a od přelomu tisíciletí zažívá renesanci na předních univerzitách, například: Johns Hopkins, Imperial College London, Curych (Tylš et al., 2014).
Farmakologie a mechanismus účinku
Psilocybin (4-fosforyloxy-N,N-dimethyltryptamin) je prodrug konvertovaná na psilocin, který má vysokou afinitu k receptorům 5-HT₂A (a dále i k 5-HT₁A/5-HT₂C). Aktivace kortikálních 5-HT₂A receptorů, zejména v prefrontálních a parietálních oblastech, je spojena se změnami funkční organizace mozkových sítí, včetně oslabení rigidních self-referenčních vzorců a zvýšení globální konektivity limbicko-asociačních okruhů, což může v terapeutickém rámci podporovat kognitivní a emoční flexibilitu (Tylš et al., 2014; Madsen et al., 2020). Na buněčné úrovni byla popsána indukce strukturální a funkční plasticity a preklinicky se ukazuje i potlačení prozánětlivých odpovědí a zvýšení IL‑10 (Ly et al., 2018).
Na periferní úrovni přehledové a experimentální práce popisují protizánětlivé účinky zprostředkované 5-HT₂A signalizací v modelových podmínkách, včetně modulace cytokinové odpovědi (Flanagan a Nichols, 2018; Nau et al., 2013; Nichols, 2020). Doplňkově jsou k dispozici laboratorní data z modelů lidské střevní tkáně naznačující protizánětlivé účinky psilocybinu v kontrolovaných podmínkách; klinická relevance pro IBD však zůstává otevřená (Robinson et al., 2023).
Fyziologické a subjektivní účinky
Po perorálním podání účinek nastupuje za 20–40 minut, trvá 4–6 hodin a je charakterizován změnami percepce, introspekcí, emoční labilitou a pocity propojenosti. Neurozobrazovací studie ukazují snížení konektivity DMN a zvýšenou synchronizaci limbicko‑senzorických oblastí, což koreluje s „rozpouštěním ega“ a perzistujícími změnami v hodnotách a tělesném uvědomění. Fyziologicky se objevuje přechodná mydriáza, mírná tachykardie a vzestup krevního tlaku – obvykle bez klinického významu (Tylš et al., 2014).
Bezpečnost a dávkování
V kontrolovaných klinických studiích je bezpečnostní profil podmíněn pečlivým screeningem, monitorovaným prostředím a strukturovanou psychoterapeutickou podporou. Akutní rizika jsou převážně psychologická (např. úzkost, panika, dysforie, derealizace/depersonalizace) a jejich pravděpodobnost významně ovlivňuje kontext, tz. „set and setting“ (Tylš et al., 2014; Griffiths et al., 2016; Ross et al., 2016). V klinickém výzkumu se používají protokoly s jednou či dvěma dávkami, často v rozmezí přibližně 20–30 mg/70 kg, v řízeném prostředí s přípravou, podporou během sezení a následnou integrací (Griffiths et al., 2016; Ross et al., 2016).
PSILOCYBINEM ASISTOVANÁ PSYCHOTERAPIE (PAP)
Princip a průběh
PAP kombinuje farmakologický účinek psilocybinu se strukturovaným psychoterapeutickým procesem, typicky v těchto fázích:
1. příprava (navázání terapeutického vztahu, práce se záměrem, psychoedukace),
2. sezení s podáním látky (bezpečné prostředí, podpůrné vedení, hudební doprovod)
3. integrace (zpracování prožitku a přenos do každodenního fungování).
Rámec „set and setting“ je klíčový (Griffiths et al., 2016; Ross et al., 2016; Tylš et al., 2014).
Role terapeuta, paměťová stopa a „vnitřní cenzura“
Je důležité zdůraznit, že účinek PAP není redukovatelný na farmakologii. Klinické popisy a fenomenologické práce naznačují, že psilocybin může dočasně zvýšit emoční otevřenost a salienci vnitřních prožitků a oslabit rigidní kontrolní strategie. V bezpečném terapeutickém rámci to může umožnit novou práci s dříve vyhýbanými tématy či autobiografickými vzpomínkami; přitom fenomenologie prožitku může souviset s přetrvávajícími psychologickými efekty (Klučková et al., 2025). Významná část variability výsledku může být dána kvalitou přípravy, vedení a integrace – nikoli pouze účinkem psilocybinu.
Psycholytické vs. psychedelické dávkování
V literatuře se někdy rozlišuje psycholytické (nižší) a psychedelické (vyšší) dávkování. Současné klinické protokoly PAP často využívají vyšší dávky v přísně strukturovaném prostředí; otázka optimální dávky, počtu sezení a míry podpory zůstává pro jednotlivé indikace otevřená (Tylš et al., 2014). Pro IBD jde zatím o výzkumnou otázku.
Klinické využití a evidence
Randomizované studie u onkologických pacientů ukazují rychlé a přetrvávající snížení úzkosti a deprese po podání psilocybinu v řízeném psychoterapeutickém kontextu (Griffiths et al., 2016; Ross et al., 2016). V somatické medicíně se pozornost přesouvá k onemocněním s významnou psychosomatickou složkou; preklinické a rané translační práce naznačují protizánětlivé, autonomně-modulační a stres-regulační účinky potenciálně relevantní i pro IBD (Flanagan a Nichols, 2018; Nau et al., 2013; Nichols, 2020; Robinson et al., 2023). Přímé klinické důkazy účinku PAP na aktivitu IBD však dosud chybí.
Mechanismus duálního účinku (pracovní hypotéza)
a) Psychologická rovina: emoční otevřenost, zpracování stresu/traumat, změna vztahu k tělu a nemoci, snížení existenciální úzkosti (Griffiths et al., 2016; Ross et al., 2016; Klučková et al., 2025).
b) Biologická rovina: aktivace 5-HT₂A → změny funkční organizace sítí a neuroplasticita; modulace autonomní rovnováhy a vybraných zánětlivých drah popsaná v experimentálních modelech (Madsen et al., 2020; Ly et al., 2018; Nau et al., 2013; Nichols, 2020).
Perspektiva pro IBD
U IBD by PAP hypoteticky mohla vést ke snížení úzkostně-depresivních symptomů, zmírnění stresové zátěže, posílení adaptivního tělesného uvědomění a zprostředkované modulaci některých psychoneuroimunitních procesů. Jde o perspektivní výzkumnou cestu.
Rizika a kontraindikace použití psilocybinu u pacientů s IBD
PAP je v kontextu IBD experimentální přístup. Bezpečnostní profil v klinických studiích je podmíněn pečlivým screeningem, kontrolovaným prostředím a strukturovanou integrační péčí (Griffiths et al., 2016; Ross et al., 2016; Tylš et al., 2014).
Obecné kontraindikace a varovné faktory typicky zahrnují osobní či rodinnou anamnézu psychotické poruchy, bipolární poruchy nebo aktuální manickou/hypomanickou symptomatologii, dále akutní suicidální krizi či výraznou dekompenzaci psychického stavu. Opatrnost je namístě také u vážnějších kardiovaskulárního onemocnění vzhledem k přechodnému vzestupu krevního tlaku a srdeční frekvence (Griffiths et al., 2016; Ross et al., 2016; Tylš et al., 2014).
Specifika relevantní pro IBD zahrnují potřebu definovat somatickou stabilitu a minimalizovat riziko zhoršení tolerance sezení. Aktivní těžký relaps se systémovými projevy (např. dehydratace, výrazná anémie, febrilie) může snižovat toleranci fyziologické zátěže. Výrazná gastrointestinální symptomatologie může zhoršit průběh sezení (nauzea, urgence, bolest), což může sekundárně zvyšovat úzkost a destabilizovat prožitek. Z těchto důvodů by rané studie u IBD měly jako primární cíle volit bezpečnost a proveditelnost, s předem stanovenými kritérii somatické stability, krizovým postupem a standardizovaným integračním protokolem.
INSPIRACE Z KARDIOLOGIE A EPIDEMIOLOGICKÉ OKÉNKO
V současné době probíhá v České republice randomizovaná studie RAFAEL (2023–2026), která zkoumá vliv PAP na regresi aterosklerózy, zánětlivé markery a autonomní rovnováhu u pacientů s kardiovaskulárním onemocněním (Clinical Trials Register, 2022). Tento výzkum vychází z předpokladu, že snížení psychosociálního stresu může mít přímý dopad na somatický stav cévní stěny.
Pokud aplikujeme stejnou logiku na idiopatické střevní záněty, argument pro využití PAP se jeví ještě naléhavěji. Jak ukazuje Tabulka 1, psychická komorbidita u pacientů s IBD není pouze výrazně zvýšená oproti běžné populaci, ale v klíčových parametrech převyšuje i zátěž pozorovanou u kardiovaskulárních onemocnění, která jsou tradičně považována za etalon psychosomatické medicíny.
Zatímco u kardiovaskulárních chorob dosahuje prevalence deprese 20,8 % a úzkosti 23,2 % (Zeng et al., 2025), u pacientů s IBD jsou tato čísla ještě více alarmující – deprese postihuje 25,2 % a úzkostné symptomy dokonce 32,1 % nemocných (Barberio et al., 2021). Vysoká prevalence úzkosti a deprese u IBD, v kombinaci s anatomicky přímým propojením skrze osu střevo–mozek a sdílenou serotonergní signalizací, poskytuje silný racionální podklad pro testování intervencí, které cílí na centrální nervový systém i imunitní regulaci současně.
Analogicky k designu studie RAFAEL lze proto navrhnout pilotní studie u IBD, které by vedle psychometrických škál sledovaly objektivní biomarkery (fekální kalprotektin, CRP, Mayo Endoskopické Skóre, SES-CD, CDAI) a autonomní regulaci (variabilita srdeční rytmu). Primárním cílem takových studií by v první fázi mělo být ověření bezpečnosti a proveditelnosti u této specifické populace.
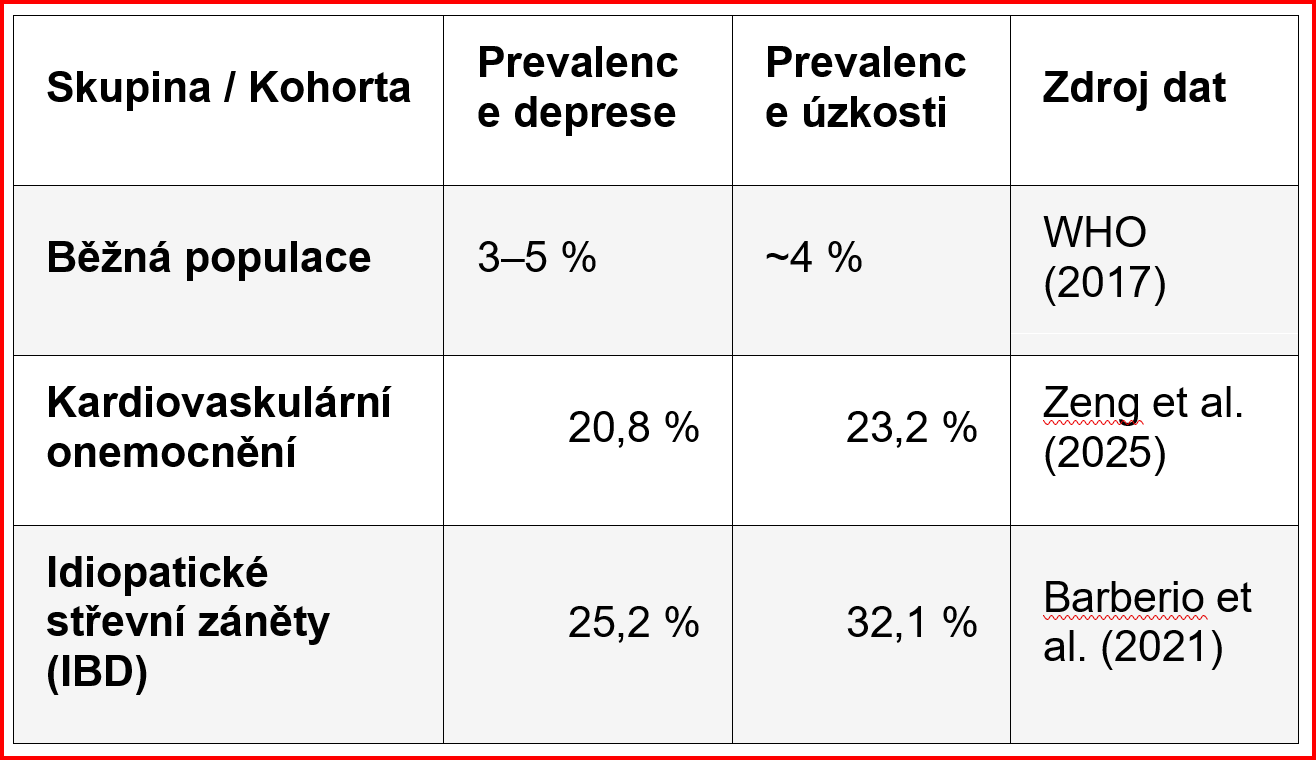
Tab. 1: Epidemiologické srovnání prevalence psychických komorbidit. Zatímco v běžné populaci se výskyt deprese a úzkosti pohybuje v řádu jednotek procent, u somatických onemocnění výrazně narůstá. Data ukazují, že pacienti s IBD vykazují vyšší míru symptomů úzkosti i deprese než pacienti s kardiovaskulárními chorobami.
ZÁVĚR
PAP je inovativní přístup propojující neurobiologické, psychologické a imunologické roviny péče. V kontextu IBD nabízí racionální, avšak zatím experimentální a neověřený potenciální terapeutický nástroj. Současné důkazy z oblasti somatické medicíny jsou omezené a přenos z psychiatrických indikací není samozřejmý. Preklinická a laboratorní data podporují hypotézu protizánětlivého potenciálu psilocybinu. Je proto nezbytné postupovat s vědeckou opatrností a dbát především na bezpečnost v dalších krocích.
LITERATURA (ABECEDNĚ)
1. Abautret-Daly Á, Dempsey E, Parra-Blanco A, Medina C, Harkin A. Gut–brain actions underlying comorbid anxiety and depression associated with IBD. Acta Neuropsychiatr. 2018;30(5):275–296.
2. Atanasova K, Lotter T, Bekrater-Bodmann R, et al. Is it a gut feeling? Bodily sensations associated with the experience of valence and arousal in patients with inflammatory bowel disease. Front Psychiatry. 2022;13:833423. doi:10.3389/fnins.2018.00049.
3. Barberio B, Zamani M, Black CJ, et al. Prevalence of symptoms of anxiety and depression in patients with inflammatory bowel disease: a systematic review and meta-analysis. Lancet Gastroenterol Hepatol. 2021;6(5):359–370.
4. Bernabeu P, van-der Hofstadt C, Rodríguez-Marín J, et al. Effectiveness of a multicomponent group psychological intervention in IBD: randomized trial. Int J Environ Res Public Health. 2021;18(10):5439.
5. Bonaz B, Bazin T, Pellissier S. The vagus nerve at the interface of the microbiota–gut–brain axis. Front Neurosci. 2018;12:49. doi:10.3389/fnins.2018.00049.
6. Bortlík M. Idiopatické střevní záněty jsou nemoci těla i duše. Česká a slovenská gastroenterologie a hepatologie. 2025;78(1).
7. Carabotti M, Scirocco A, Maselli MA, Severi C. The gut–brain axis: interactions between enteric microbiota, central and enteric nervous systems. Ann Gastroenterol. 2015;28(2):203–209.
8. Clinical Trials Register. Regression of atherosclerosis induced by life changing experience with psilocybin (RAFAEL). EudraCT 2022-003381-21. Dostupné z: https://www.clinicaltrialsregister.eu/ctr-search/trial/2022-003381-21/CZ (cit. 16.12.2025).
9. Costa Santos MP, Gomes C, Torres J. Familial and ethnic risk in inflammatory bowel disease. Ann Gastroenterol. 2018;31(1):14–23. doi:10.20524/aog.2017.0208.
10. Ferreira C, Pereira J, Skvarc D, et al. Randomized controlled trial of an ACT- and compassion-based group intervention for persons with IBD (LIFEwithIBD). Front Psychol. 2024;15:1367913.
11. Flanagan TW, Nichols CD. Psychedelics as anti-inflammatory agents. Int Rev Psychiatry. 2018;30(4):363–375.
12. Gao K, Mu CL, Farzi A, Zhu WY. Tryptophan metabolism: a link between the gut microbiota and brain. Adv Nutr. 2020;11(3):709–723.
13. Ge L, Li Y, Chen X, et al. Psychological stress in inflammatory bowel disease: psychoneuroimmunological insights into bidirectional gut–brain communications. Front Immunol. 2022;13:1016578. doi:10.3389/fimmu.2022.1016578.
14. Ghia JE, Blennerhassett P, Collins SM. Impaired parasympathetic function increases susceptibility to inflammatory bowel disease in a mouse model of depression. J Clin Invest. 2008;118(6):2209–2218. doi:10.1172/JCI32849.
15. Griffiths RR, Johnson MW, Carducci MA, et al. Psilocybin produces substantial and sustained decreases in depression and anxiety in patients with life-threatening cancer: randomized double-blind trial. J Psychopharmacol. 2016;30(12):1181–1197.
16. Hu S, Wang W, Wang Z, et al. Depression and anxiety disorders in patients with IBD: prevalence, risk factors, and management. Front Psychiatry. 2021;12:714057.
17. Irving P, Barrett K, Nijher M, de Lusignan S. Prevalence of depression and anxiety in people with IBD and associated healthcare use: population-based cohort study. Evid Based Ment Health. 2021;24(3):102–109.
18. Kim JS, Park J, Lee S, et al. Risk of anxiety and depression in patients with inflammatory bowel disease: a nationwide, population-based study. J Crohns Colitis. 2019;13(6):707–715.
19. Klučková T, Nikolič M, Tylš F, et al. The phenomenology of psilocybin’s experience mediates subsequent persistent psychological effects. Pharmacol Rep. 2025;77(4):1024–1039.
20. Ly C, Greb AC, Cameron LP, et al. Psychedelics promote structural and functional neural plasticity. Cell Rep. 2018;23(11):3170–3182.
21. Madsen KM, Fisher PM, Páleníček T, Kuchař M, Knudsen GM. A single psilocybin dose is associated with long-term increased mindfulness, preceded by proportional change in neocortical 5-HT2A receptor binding. Eur Neuropsychopharmacol. 2020;33:71–80.
22. Mayer EA. Gut feelings: the emerging biology of gut–brain communication. Nat Rev Neurosci. 2011;12(8):453–466.
23. Mikocka-Walus A, Knowles SR, Keefer L, Graff L. Controversies revisited: a systematic review of the comorbidity of depression and anxiety with IBD. Inflamm Bowel Dis. 2016;22(3):752–762.
24. Mináriková M, et al. Nejčastější duševní onemocnění u pacientů s idiopatickými střevními záněty. Česká a slovenská gastroenterologie a hepatologie. 2025;79(1).
25. Nau F Jr, Yu B, Martin D, Nichols CD. Serotonin 5-HT2A receptor activation blocks TNF-α-mediated inflammation in vivo. PLoS One. 2013;8(10):e75426.
26. Neuendorf R, Harding A, Stello N, Hanes D, Wahbeh H. Depression and anxiety in patients with inflammatory bowel disease: a systematic review. J Psychosom Res. 2016;87:70–80.
27. Nichols CD. Psychedelics as potent anti-inflammatory therapeutics. Brain Behav Immun. 2020;87:548–550.
28. Paulides E, Boukema I, van der Woude CJ, de Boer NKH. The effect of psychotherapy on quality of life in IBD patients: a systematic review. Inflamm Bowel Dis. 2021;27(5):711–724.
29. Petrik M, Palmer B, Khoruts A, Vaughn BP. Psychological features in the inflammatory bowel disease–irritable bowel syndrome overlap: developing a preliminary understanding of cognitive and behavioral factors. Crohns Colitis 360. 2021;3(3):otab061. doi:10.1093/crocol/otab061.
30. Ross S, Bossis A, Guss J, et al. Rapid and sustained symptom reduction following psilocybin treatment for anxiety and depression in patients with life-threatening cancer: randomized controlled trial. J Psychopharmacol. 2016;30(12):1165–1180.
31. Sun Y, Li L, Xie R, et al. Stress triggers flare of inflammatory bowel disease in children and adults. Front Pediatr. 2019;7:432. doi:10.3389/fped.2019.00432.
32. Tarar ZI, Zafar MU, Farooq U, et al. Burden of depression and anxiety among patients with inflammatory bowel disease: a nationwide analysis. Int J Colorectal Dis. 2022;37(2):313–321.
33. Tiles-Sar N, Neuser J, de Sordi D, et al. Psychological interventions for treatment of inflammatory bowel disease. Cochrane Database Syst Rev. 2025;Issue 4:CD006913.
34. Tylš F, Páleníček T, Horáček J. Psilocybin—summary of knowledge and new perspectives. Eur Neuropsychopharmacol. 2014;24(3):342–356.
35. Ungaro R, Mehandru S, Allen PB, Peyrin-Biroulet L, Colombel JF. Ulcerative colitis. Lancet. 2017;389(10080):1756–1770.
36. Wang L, Liang C, Chen P, et al. Effect of antidepressants on psychological comorbidities, disease activity and QoL in IBD: systematic review and meta-analysis. Ther Adv Gastroenterol. 2023;16:17562848231155022.
37. Weston F, Carter B, Powell N, Young AH, Moulton CD. Antidepressant treatment in inflammatory bowel disease: a systematic review and meta-analysis. Eur J Gastroenterol Hepatol. 2024;36(7):850–860.
38. Wohlberg RH, Kvasnovsky C, Thayer A, et al. The Computerized Adaptive Test for Mental Health (CAT-MH) is an effective screening tool for depression and anxiety in inflammatory bowel disease. Inflamm Bowel Dis. 2020;26(8):1233–1240. doi:10.1093/ibd/izz249.
39. World Health Organization. Depression and other common mental disorders: global health estimates. Geneva: World Health Organization; 2017. Dostupné z: https://apps.who.int/iris/handle/10665/254610
40. Zeng J, Qiu Y, Yang C, et al. Cardiovascular diseases and depression: A meta-analysis and Mendelian randomization analysis. Molecular Psychiatry. 2025;30:4234–4246. doi:10.1038/s41380-025-03003-2.
Do redakce přišlo 14.11.1025
Po recenzním řízení zařazeno k tisku 15.1.2026
Konflikt zájmů není znám.
AUTOŘI:


 1. autor: MUDr. Jakub Figueroa – Psychiatrická klinika, Fakultní nemocnice Plzeň, figueroaj@fnplzen.cz
1. autor: MUDr. Jakub Figueroa – Psychiatrická klinika, Fakultní nemocnice Plzeň, figueroaj@fnplzen.cz
Korespondenční autor: MUDr. Santóš Samuel Rajpoot – IBD Centrum a gastroenterologie Turnov, Krajská nemocnice Liberec, a.s., santosrajpoot@gmail.com
Odborný konzultant: prim. MUDr. Lenka Nedbalová – IBD Centrum a gastroenterologie Turnov, Krajská nemocnice Liberec, a.s., lenka.nedbalova@nemlib.cz
Spoluautor posteru: Martin Vašek – student 5. ročníku 3. lékařské fakulty UK




